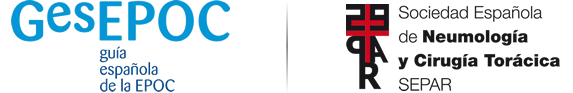Tratamiento
Las pautas de tratamiento deberán ser adecuadas a cada paciente en función de los posibles factores desencadenantes, su gravedad y los RT identificados. En este sentido, se distinguen dos escenarios de tratamiento, el ambulatorio y el hospitalario (figura 4). Más del 80% de las agudizaciones se manejan de forma ambulatoria (43). La tabla 5 resume las principales preguntas PICO referidas al tratamiento del SAE.
El tratamiento broncodilatador destinado al alivio inmediato de los síntomas se considera esencial para todos los pacientes, mientras que el uso de antibióticos, corticoides sistémicos, oxigenoterapia, ventilación asistida o el tratamiento de la propia comorbilidad variará en función de la gravedad o de los posibles RT del SAE (figura 4, tabla 6).
Figura 4. Tratamiento farmacológico del síndrome de agudización de la EPOC. RT: rasgo tratable; BDAC: broncodilatadores de acción corta; SAMA: antimuscarínicos de acción corta; SABA: β2-agonistas adrenérgicos de acción corta.
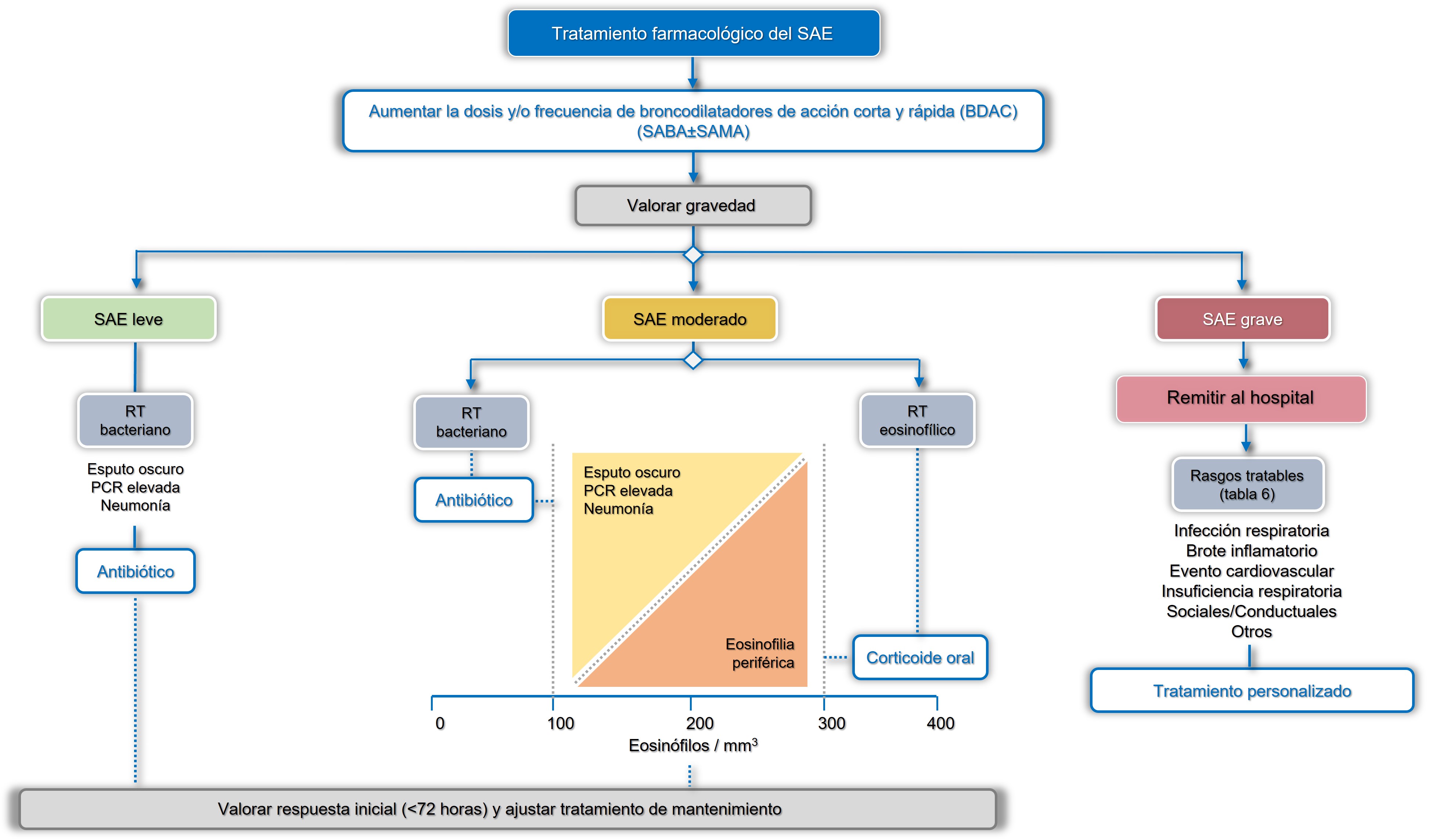
Tabla 6. Rasgos tratables del síndrome de agudización de la EPOC
RT: rasgo tratable; Rx: radiografía; TC: tomografía computerizada. PCR: proteína C-reactiva; NT-proBNP: fracción N-Terminal del propéptido natriurétrico cerebral o tipo B; ARA-II: Antagonistas del receptor de la angiotensina II; IECAS: inhibidor del enzima convertidor de la angiotensina.
Tratamiento farmacológico
Broncodilatadores
En el SAE de cualquier intensidad, la principal intervención consiste en la optimización de la broncodilatación, aumentando la dosis o la frecuencia de los broncodilatadores (44). Los broncodilatadores de acción corta son de elección para el tratamiento del SAE. Se deberán emplear fármacos de acción rápida como los β2-agonistas (salbutamol y terbutalina), y se puede añadir al tratamiento si fuera necesario un anticolinérgico de acción corta (ipratropio).
Para administrar los fármacos inhalados durante la agudización, se pueden utilizar dispositivos presurizados de dosis medida (pMDI) con cámara de inhalación o nebulizadores. Una revisión sistemática sobre las formas de administración de los broncodilatadores de acción corta concluye que cuando la técnica inhalatoria es buena, no hay diferencias significativas sobre el FEV1 entre los cartuchos presurizados con o sin cámara espaciadora, y los nebulizadores (45).
Las dosis recomendadas son para el caso del salbutamol de 400-600 µg/4-6 h (4-6 inhalaciones/ 4-6h) o terbutalina 500-1.000 µg/ 4-6h (1-2 inhalaciones/6h) y en el caso de ipratropio de 80-120 µg/4-6h (4-6 inhalaciones c/4-6h). En el caso de utilizar la medicación nebulizada la pauta será de 2,5-5 mg de salbutamol y/o 0,5-1 mg de ipratropio cada 4-6 horas.
Los broncodilatadores de larda duración (BDLD) constituyen el tratamiento de base de la EPOC y su eficacia en el SAE no está suficientemente documentada (46). Sin embargo, es importante recordar que si el paciente ya utiliza BDLD para el control de su enfermedad de base, éstos no deberán suspenderse durante el tratamiento del SAE ambulatorio.
Antibióticos
En las agudizaciones ambulatorias y en los pacientes ingresados, el uso de antibióticos reduce el riesgo de fracaso terapéutico e incrementa el tiempo hasta la siguiente agudización, sin afectar a la calidad de vida relacionada con la salud (CVRS), las recurrencias o la mortalidad (47-49). En los casos que precisan ingreso en la Unidad de Cuidados Intensivos (UCI) el tratamiento antibiótico se ha asociado a una reducción significativa de la mortalidad por cualquier causa, a menor fracaso terapéutico y una menor duración de la estancia hospitalaria (47,50). En general, se sugiere el empleo de antibióticos durante un SAE ambulatorio u hospitalario, recomendándose especialmente su administración en todos los pacientes que precisen ingreso en UCI (tabla 5, suplemento 1). Muchos de los SAEs tratados con placebo evolucionan favorablemente, lo que sugiere que el antibiótico no siempre es necesario. La administración de antibiótico estará especialmente indicada ante un cambio en el color del esputo (de mucoso a oscuro) (47-49); cuando el paciente requiere asistencia ventilatoria tanto invasiva como no invasiva (50) y en los casos con PCR elevada (≥20 mg/dL), aunque el aspecto del esputo no sea concluyente (30,31). También se recomienda el empleo de antibióticos en todos los pacientes con SAE que cursen con neumonía, de acuerdo con las recomendaciones que establecen las guías de práctica clínica de la neumonía (33,34,51)
La tabla 7 indica cuáles son los principales antibióticos para considerar durante el SAE. Esta elección dependerá del conocimiento de las especies bacterianas involucradas, resistencias antibióticas locales, de la gravedad de la propia agudización y del riesgo de infección por Pseudomonas aeruginosa. Este riesgo se define por el uso de 4 ó más ciclos de tratamiento antibiótico en el último año, una función pulmonar con un FEV1<50% del predicho, la presencia de bronquiectasias significativas o el aislamiento previo de Pseudomonas en esputo en fase estable o en una agudización previa (1,52,53).
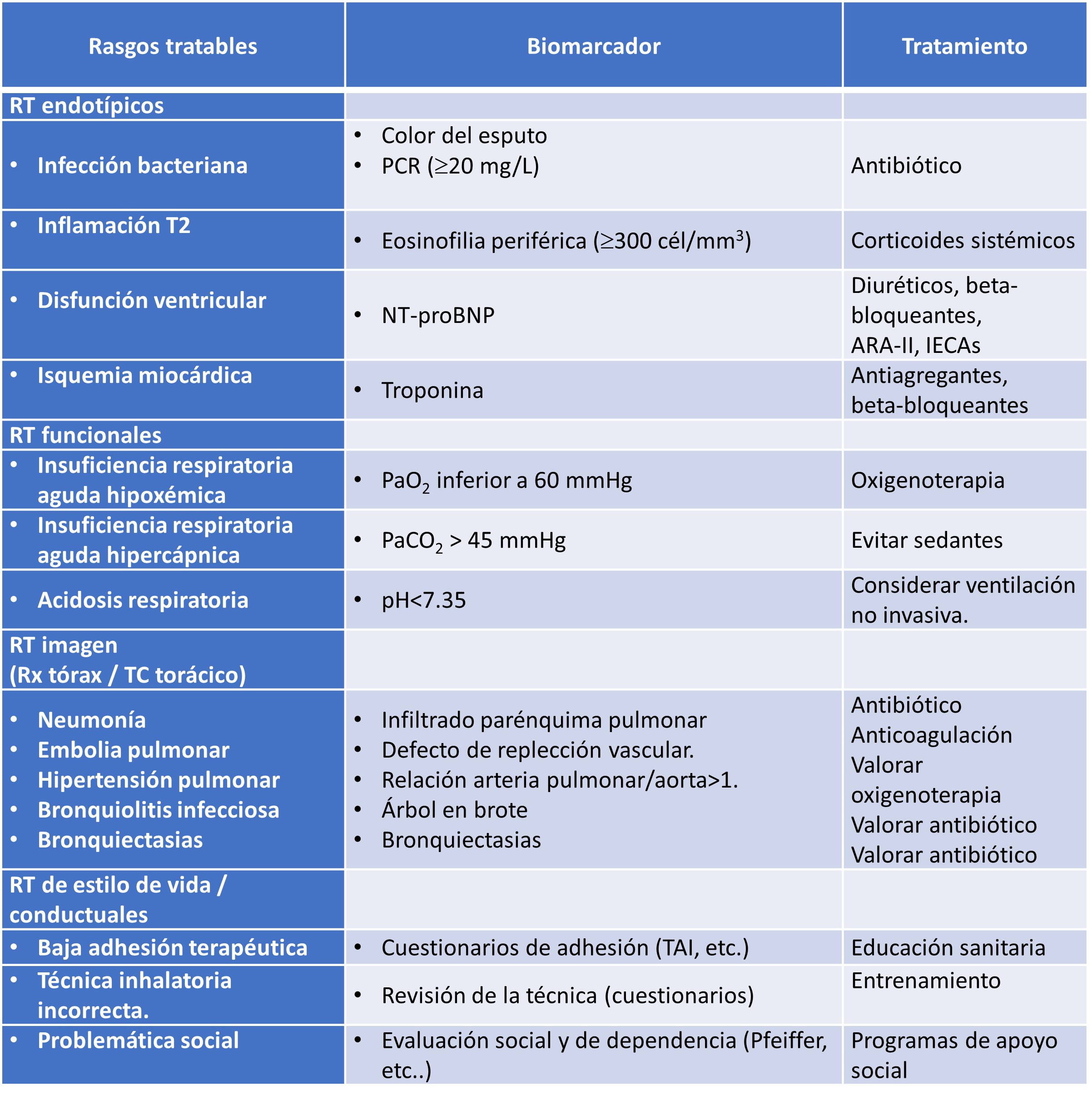
Tabla 7. Recomendación sobre el uso de antibióticos en el SAE
(1) La administración de medicamentos y alimentos de los Estados Unidos (FDA) y la Agencia Europea de Medicamentos (EMA) recomiendan evitar fluoroquinolonas si existe alternativa terapéutica debido a sus efectos adversos.
(2) Piperacilina-tazobactam, ceftazidima, cefepima, meropenem, ceftolozano-tazobactam, ceftazidima-avibactam.
(3) Ciprofloacino 500-750 mg cada 12 horas o levofloxacino 500 mg cada 12 horas.
Corticoides sistémicos
Los corticoides sistémicos han demostrado acelerar la recuperación de los síntomas, mejorar la función pulmonar y disminuir los fracasos terapéuticos, aunque sin reducir la mortalidad (47,54). Sin embargo, estudios recientes indican que estos fármacos pueden ser menos eficaces en pacientes con cifras bajas de eosinófilos en sangre (55,56). De acuerdo con la revisión sistemática realizada por esta guía y con carácter general, se recomienda el empleo de corticoides orales en pacientes con SAE grave o muy grave y se sugiere su empleo para el SAE moderado (tabla 5, suplemento 1). La eficacia de estos fármacos en el SAE es mayor en pacientes con recuento de eosinófilos ³ 300 células/mm3. La dosis recomendada es de 0,5 mg/kg/dia de prednisona o equivalente durante un máximo de 5 días en el SAE moderado y un máximo de 14 días en el grave o muy grave (47,57). Aunque no se han observado diferencias entre la administración intravenosa o la oral (47), la vía parenteral es preferible para los SAE muy graves.
Profilaxis de la enfermedad tromboembólica venosa (ETV)
El SAE graves o muy grave de la EPOC comportan un riesgo elevado de ETV, por lo que se recomienda el uso de heparinas de bajo peso molecular a dosis profilácticas de alto riesgo (58). En el SAE moderado, en el que el paciente permanece encamado o inactivo 3 o más días, también está indicado su uso.
Optimizar el tratamiento de la comorbilidad
En la EPOC es frecuente la coexistencia de distintas comorbilidades como la hipertensión arterial, cardiopatía isquémica, arritmias, insuficiencia cardíaca o diabetes. Por ello será necesario optimizar su tratamiento, de acuerdo con las recomendaciones establecidas por las guías de práctica clínica específicas. En pacientes cardiópatas, tanto los β2-agonistas como los anticolinérgicos de acción corta se han asociado a un incremento de arritmias, por lo que se debe ser cauteloso con la dosis empleada, especialmente con los dispositivos nebulizados (59).
Tratamiento no farmacológico
Oxigenoterapia
La administración de oxígeno suplementario se considera una de las piezas clave del tratamiento del SAE grave de la EPOC que cursa con insuficiencia respiratoria. El objetivo de la oxigenoterapia es alcanzar una SaO2 entre 88-92%. Sin embargo, la administración de oxígeno debe realizarse de forma controlada, ya que en algunos pacientes el principal estímulo del centro respiratorio depende del grado de hipoxemia más que del habitual estímulo hipercápnico. La administración de oxígeno de forma incontrolada puede producir supresión del estímulo respiratorio, carbonarcosis e incluso parada respiratoria. En la práctica clínica, se deben administrar bajas concentraciones inspiratorias de oxígeno, bien 24% o 28%, mediante mascarillas de alto flujo tipo Venturi o mediante gafas nasales a bajos flujos de 2-4 L/min.
Oxigenoterapia de alto flujo (OAF)
La terapia de alto flujo permite suministrar gas a flujos altos (hasta de 60 L/min) con proporciones variables de aire y oxígeno mediante una cánula nasal, con el gas administrado a nivel de temperatura y humedad ideales (37ºC y 100% de humedad relativa). En el SAE la OAF ha demostrado mejorar la oxigenación y la ventilación, disminuyendo la hipercapnia y mejorando la CVRS (60-62). Algunos ensayos no controlados y un ensayo aleatorizado reciente de no inferioridad han comparado el uso de la OAF frente a la ventilación no invasiva (VNI) en pacientes con EPOC con acidosis leves-moderadas (pH: 7,25 – 7,35), sin encontrar diferencias significativas, aunque con mejor tolerancia para el OAF (63-65). A pesar de estos potenciales beneficios, se necesita incorporar más evidencia para poder establecer las recomendaciones específicas de uso en el SAE.
Ventilación asistida
En los casos donde existe un fracaso ventilatorio grave, con alteración del nivel de consciencia o acidosis respiratoria, a pesar de tratamiento médico óptimo, se debe considerar el empleo de soporte ventilatorio (1). La ventilación mecánica puede ser administrada de forma no invasiva o invasiva (VI).
Ventilación mecánica no invasiva
En pacientes con fallo respiratorio agudo hipercápnico la VNI disminuye la mortalidad, la necesidad de intubación y las complicaciones del tratamiento respecto al tratamiento habitual sin soporte ventilatorio. También disminuye la estancia hospitalaria y la estancia en la unidad de cuidados intensivos (1,47,66). La tabla 8 señala cuáles son las indicaciones y contraindicaciones de la VNI.
Tabla 8. Indicaciones y contraindicaciones relativas de la ventilación no invasiva (VNI).
Ventilación mecánica invasiva
Debe considerarse en los casos de parada respiratoria, intolerancia o fracaso de la VNI, empeoramiento de la acidosis respiratoria (pH<7,25), inestabilidad hemodinámica o disminución del nivel de consciencia, que no mejora con tratamiento correcto (1).
Rehabilitación respiratoria precoz
En pacientes hospitalizados por una agudización de EPOC, los programas de rehabilitación pulmonar temprana reducen los reingresos, mejora la CVRS y la capacidad de ejercicio (67). No obstante, estos resultados son variables según el momento de inicio del programa. La disminución de reingresos únicamente es significativa para programas iniciados tras 4 semanas del alta hospitalaria.